PROSES EKSTRAKSI TEMBAGA
Tembaga (Cu) berasal dari bahasa yunani
Kypros atau Siprus berarti merah. Tembaga adalah salah satu dari dua logam
dibumi selain emas yang berwarna merah atau kekuningan, mempunyai nomor Atom 29
dengan kepadatan 8, 92g/ cm3 . Tembaga murni mencair pada suhu 1083° C dan akan
menjadi uap atau mendidih pada suhu 2567° C pada tekanan normal.
Besi yang terbentuk di dalam tanur tiup masih mengandung pengotor dan bersifat cukup rapuh. Besi ini disebut juga besi gubal (pig iron). Besi gubal mengandung sekitar 3 – 4% C, 2% Si, dan sejumlah pengotor lain seperti P dan S. Besi gubal dapat dicetak langsung menjadi besi tuang (cast iron).
Bijih tembaga yang sangat penting
berupa sulfida seperti kalkosit dan kalkopirit. Tembaga di alam terdapat
sebagai: sulfida, seperti chalcopite, bronit, chalcocite, covelite dan oksida,
seperti cuprite, ferronite. Proses ekstraksi mineral tembaga menjadi tembaga
batang dikenal 2 macan cara, yaitu:
A. Phyrometalurgi
Adalah suatu proses pengolahan
mineral dengan dasar panas dengan pengolahan tembaga melalui suatu proses yang
bertujuan untuk mengubah pengotor senyawa Sulfida menjadi Oksida atau disebut
dengan proses Roasting. Reaksinya yaitu:
CuFeS2+ 9O2
menjadi 2Cu2S+ 2Fe2O3+ 6SO2
Berdasarkan reaksi diatas, proses
Roasting bertujuan untuk mengubah Besi Sulfida menjadi Besi Oksida sedangkan
Tembaga tetap Sulfida. Diubahnya besi sulfida menjadi besi oksida adalah agar
pada proses selanjutnya yaitu smelting atau peleburan, tembaga sulfida akan
mencair meninggalkan besi oksida yang bertitik cair lebih tinggi dan akan
ditinggalkan sebagai terak pengotor, sedangkan tembaga yang telah mencair akan
turun kebawah karena berat jenis tembaga yang lebih tinggi dari besi oksida.
Adapun urutan prosesnya sebagai
berikut:
1. Bijih tembaga dihaluskan dengan alat peremuk batuan
2. Bijih dicampur air sehingga
terbentuk slurry
3. Slurry dimasukkan ke tangki sel flotasi dengan tujuan pemisahan dari
mineral pengotor
4.
Diperoleh konsentrat
Cu dalam bentuk Cu dengan kadar tinggi
5.
Diproses lanjut dalam
pabrik pengawa-airan ( dewatering plant) untuk menghilangkan air dengan:
penyaring putar dan pengeringan sampai di dapat konsentrat Cu yang kering
6.
Roasting atau
pemanggangan bertujuan untuk proses reduksi pengotor
7. Ekstraksi tembaga murni dari konsentrat tembaga dengan dengan:
prometalurgi dan elektrolisis ( dengan arus listrik)
B. Hidrometalurgi
Hidrometalurgi adalah suatu
proses pengolahan tembaga dari batuan alam dengan berdasar pada air sebagai
pengolahnya, namun maksud air adalah bukan air biasa melainkan air yang telah
dicampur dengan suatu asam tertentu sebagai reduktor.
Pada proses ini dipakai suatu
asam sebagai reduktor yaitu asam sulfat ( H2SO4) yang
mudah didapatkan dan rendah biaya pengolahan. Dipakainya asam sulfat sebagai
pereduktor adalah bertujuan untuk membentuk tembaga sulfat ( CuSO4.5H2O)
. Tembaga adalah suatu unsur yang sangat mudah membentuk sulfida. Maka dari itu
asam sulfat dipakai sebagai pilihan.
Adapun prosesnya adalah sebagai
berikut :
·
Mula-mula batuan
tembaga dihancurkan hingga menjadi halus sampai mess tertentu.
·
Selanjutnya tempatkan
pada suatu tabung yang terbuat dari bahan tahan asam ( plastik, fiber, dll)
lalu ditambah air dengan ukuran tertentu.
·
Kemudian tambahkan
asam sulfat pekat sambil diaduk agar terbentuk larutan tembaga sulfat ( CuSO4.5H2O)
.
·
Setelah terbentuk
larutan tembaga sulfat pindahkan pada suatu tabung elektrolisis yang bertujuan
untuk mengambil ion tembaga dari larutan tembaga sulfat yang terbentuk pada
proses pengasaman.
·
Secara bertahap ambil
tembaga yang mene mpel pada katoda, dan tembaga hasil dari katoda adalah
tembaga murni.
·
Selanjutnya tembaga
hasil dari katoda siap untuk proses peleburan pada tungku peleburan tembaga
yang mampu menghasilkan suhu 1300° C.
2. PROSES
EKSTRAKSI BESI
Besi
merupakan unsur kimia yang mempunyai
sifat-sifat kuat, liat, keras, penghantar listrik dan panas, serta mempunyai
titik cair tinggi. Bijih besi ditemukan dengan cara penambangan yang terdapat
dalam keadaan murni atau bercampur. Bijih besi yang ditemukan dalam keadaan
murni yaitu emas, perak, bismut, platina, dan ada yang bercampur dengan
unsur-unsur seperti karbon, sulfur, fosfor, silikon, serta kotoran seperti
tanah liat, pasir, dan tanah.
Besi adalah logam yang
berasal dari bijih besi (tambang) yang banyak digunakan untuk kehidupan manusia
sehari-hari. Dalam tabel
periodik, besi mempunyai simbol Fe dan nomor atom 26.
Besi juga mempunyai nilai ekonomis yang tinggi. Besi dapat diekstraksi dari bijih besi yang mengandung senyawa
besi seperti hematite (Fe2O3), limonit (2Fe2O3 3H2O),
magnetit (Fe3O4), dan siderit (FeCO3). Proses
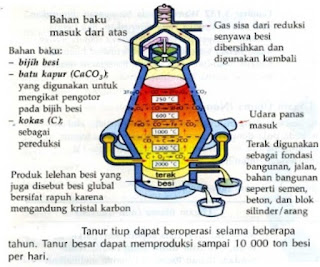
ekstraksi dilakukan dalam tungku yang disebut tanur tiup (blast furnace) dengan
menggunakan metode reduksi. Simak proses ekstraksinya berikut ini. Berikut
tahapan ekstraksi Fe dari bijih besi:
·
Bijih besi, batu kapur (CaCO3),
dan kokas (C) dimasukkan dari bagian atas tanur.
·
Kemudian, udara panas
ditiupkan ke bagian bawah tungku agar C bereaksi dengan OZ membentuk CO2.
C(s) +O2(S) à CO2(S)
Gas CO2 yang
terbentuk selanjutnya akan bergerak ke atas dan lebih lanjut dengan C untuk
membentuk CO. Reaksi ini bersifi endotermik, sehingga terjadi sedikit penurunan
suhu proses.
CO2(g) + C(s)
à
2CO(S)
Produk
reaksi yakni gas CO kemudian bergerak naik dan mulai mereduksi senyawa-senyawa
besi pada bijih besi.
3Fe2O3(5)
+ CO(g) à 4 2Fe3O4(s)
+ CO2(g)
Fe3O4(s)
+ CO(g) à 3FeO(6) + CO2(g)
FeO(s) + CO(g) à Fe(s) + CO2(g)
Reaksi
keseluruhannya dapat ditulis sebagai berikut:
Fe2O3(s) +
3CO(s) à 2Fe(l) +
3CO2(g)
Fe yang
terbentuk akan mengalir dan berkumpul di bawah. Karena suhu di bawah tinggi
sekitar 2000°C, Fe akan berada dalam bentuk lelehannya.
·
Sementara itu, CaCO3 dalam
tanur akan terurai menjadi CaO.
CaCO3(s)—>
CaO(s) + CO2(g)
·
CaO yang terbentuk akan
bereaksi dengan pengotor yang bersifat asam yang ada dalam bijih besi, seperti
pasir silika. Reaksi ini menghasilkan senyawa dengan titik didih rendah yang
disebut terak (slag).
CaO(S) + SiO2(s)
à CaSiO3(l)
·
Lelehan terak kemudian akan
mengalir ke bagian bawah tanur. Karena kerapatan lelehan terak yang lebih
rendah dibandingkan lelehan besi, maka lelehan terak berada di atas lelehan
besi sehingga keduanya dapat dikeluarkan secara terpisah. (Secara tidak
langsung, lelehan terak ini melindungi lelehan besi dari teroksidasi kembali)
Besi yang terbentuk di dalam tanur tiup masih mengandung pengotor dan bersifat cukup rapuh. Besi ini disebut juga besi gubal (pig iron). Besi gubal mengandung sekitar 3 – 4% C, 2% Si, dan sejumlah pengotor lain seperti P dan S. Besi gubal dapat dicetak langsung menjadi besi tuang (cast iron).
Komentar